アルキンとは
アルキンとは炭素Cと水素Hだけでできている炭化水素の中で、三重結合C≡C結合を1つもつ鎖状のものをいいます。鎖状なので環は持ちません。
アルカンからHを2つ取り二重結合を作ってアルケンにし、さらにアルケンからHを2つとって三重結合を作りアルキンにしたと考えれば、アルキンの一般式は次のようになります。
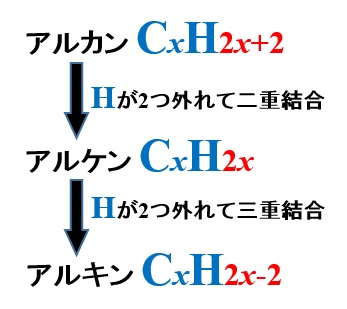
アルキンの名称と構造式
アルキンの名前は、アルカンalkaneのaneをyneに変えればよいです。アルカンのエタンC2H6がアルキンのエチンC2H2になった場合は、エチンよりもアセチレンと呼ぶことが多いようです。
アセチレン(エチン) C2H2
アルカンのエタンCH4が三重結合をもった構造です。エチンよりアセチレンと呼ぶことが多いようです。アセチレンを酸素とともに燃焼させると、酸素アセチレン炎という高温の炎になります。この高温の炎で鉄を溶接したりしています。

結合の距離Cから次のCまでの距離は、結合が増えるごとに距離が短くなります。
プロピン(メチルアセチレン)C3H4
メチルアセチレンよりもプロピンと呼ぶことが多いようです。アセチレンに炭素Cが1つ増えた構造です。増えたCにメチル基になるので、メチルアセチレンと呼びます。メチル基のH以外は同一平面上にあります。

ブチンC4H6
ブチンには、三重結合が一番外側(1番目)の炭素Cにある1-ブチンと真ん中(2番目)の炭素Cにある2-ブチンの構造異性体があります。
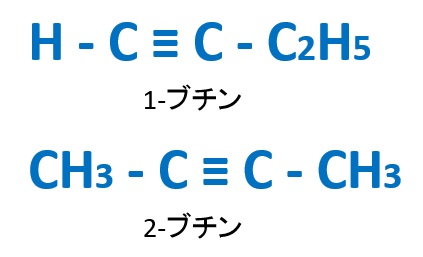
以上がアルキンです。次はアセチレンの製法と反応です。
アセチレンの製法
アルキンのアセチレンCH≡CHは、実験室では、炭酸カルシウム(カーバイド)CaC2に水H2Oを加えて発生させることができます。また、アルケンと同様に、工業的にはアルカンの熱分解で得ることができます。
CaC2 + 2H2O → C2H2 + Ca(OH)2
アルキンの化学的性質
アルキンの持つ三重結合C≡Cは、アルケンの二重結合と同じように反応性が高く、C=C結合と同じような反応を見せます。
付加反応
アルキンのC≡C結合のうち、2本は切れやすい結合になっているので、次のように付加反応を起こします。条件を整えれば、1回目の付加反応で止めることもできます。
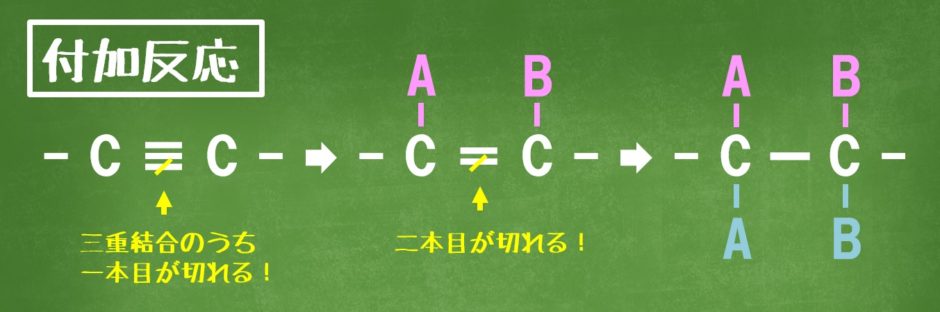
臭素の付加
臭素Br2水中にアセチレンを通すと、アルケンのC=C結合と同じように、C≡C結合に赤褐色のBr2が付加し、無色の化合物になります。このとき触媒は必要ありません。
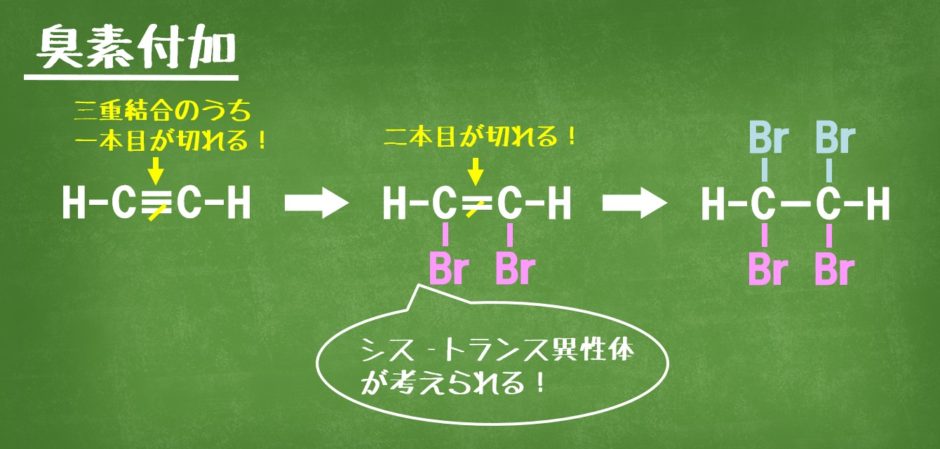
臭素Br2の付加では、Br2の赤褐色が消えるので、C=C結合の検出だけでなく、C≡Cの検出にも用いられます。
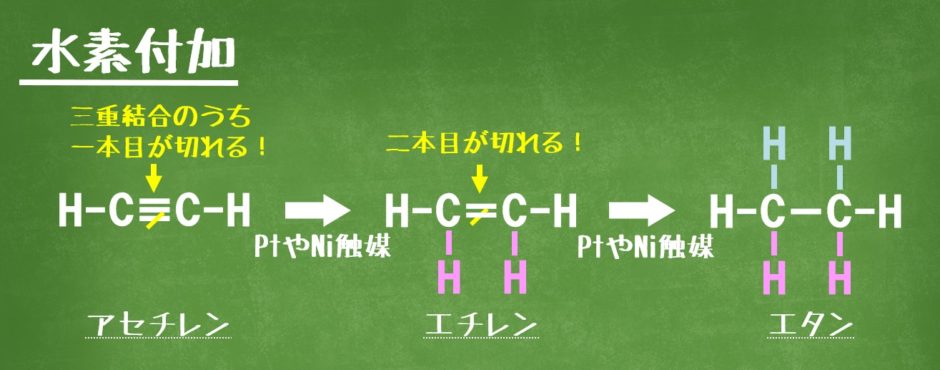
水素の付加
白金PtやニッケルNiなどの触媒を使い、水素H2を付加することができます。アセチレンCH≡CHからエチレンCH2=CH2、さらにエタンCH3-CH3になります。
酸の付加
塩化水素HCl、酢酸CH3COOH、シアン化水素HCNなどのHXで表される酸を付加させると、ビニル基が残り、ビニル化合物を生成します。このとき触媒が必要になります。
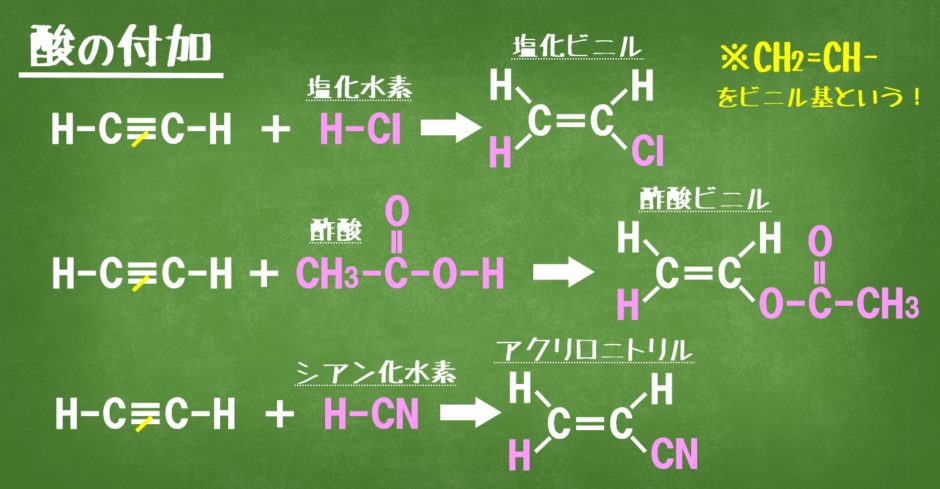
ビニル化合物は付加重合して高分子になります。塩化ビニルはポリ塩化ビニル、酢酸ビニルはポリ酢酸ビニル、アクリロニトリルはポリアクリロニトリルになります。
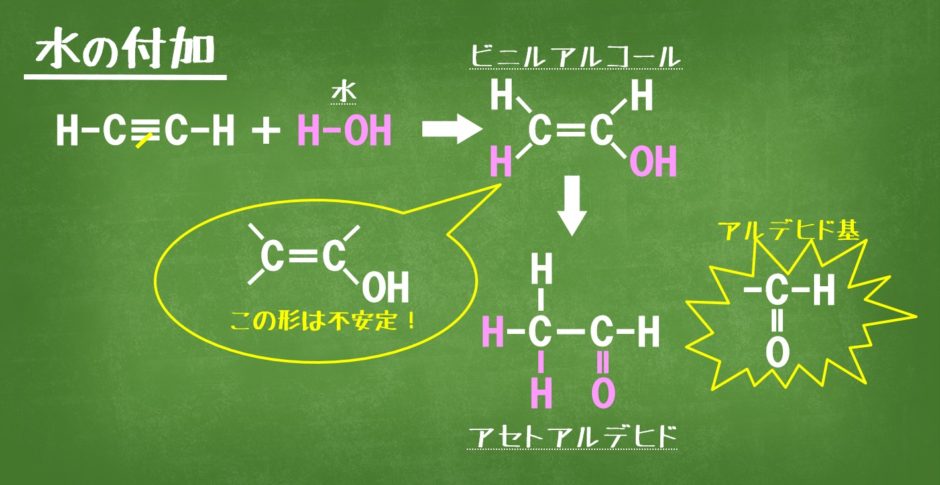
水の付加
水銀塩HgSO4(触媒)水溶液にアセチレンを通すと、水が付加されて、ビニルアルコールを生じます。しかし、ビニルアルコールは不安定なので、すぐに異性体のアセトアルデヒドに変化してしまいます。
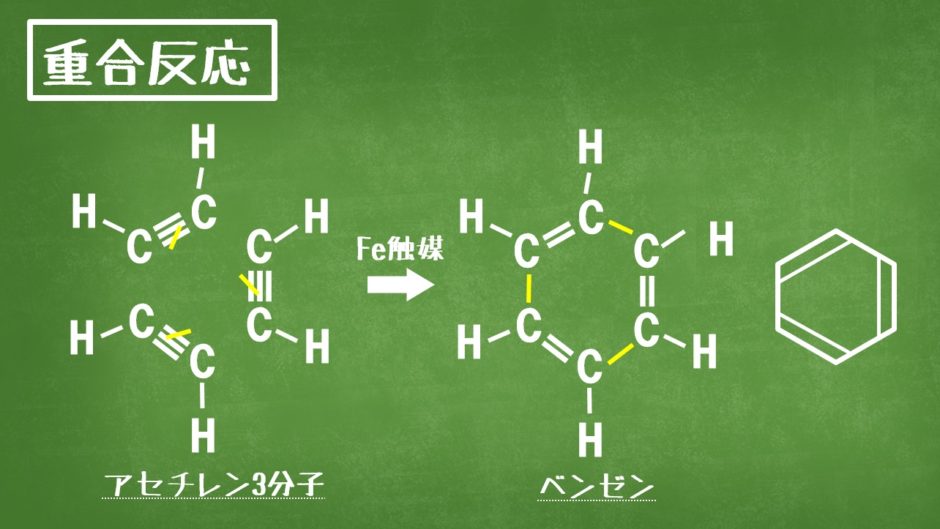
重合反応
同じ分子が次々と結合することを重合といいます。アセチレンCH≡CHを、赤くなるまで加熱した鉄つまり赤熱した鉄などの触媒に触れさせると、アセチレン3分子が重合してベンゼンC6H6が生成します。
全て重要ですので、しっかりと覚えていきましょう!最後にもう一度復習です。
今日のまとめ
■アセチレンの製法
CaC2 + 2H2O → C2H2 + Ca(OH)2
■付加反応
臭素Br2の付加、水素H2の付加、酸HXの付加、水H2Oの付加反応
■重合反応
アセチレンCH≡CH3分子が重合してベンゼンC6H6が生じる


コメント