【2024年度】九州産業高校入試対策問題(解答・ポイント解説付)です。
九産大付属九州産業高校と同じように普通科に3つないし4つのクラス、各学校によって呼び名は違いますが「スーパ-特進」「特進、準特進」「進学クラス、一般進学」など分かれている高校を受験する人も解いてみてください。
(例)九産大付属九州高校、東福岡高校、福岡工大城東高校、福岡舞鶴高校、福岡大若葉、中村学園女子高校、筑陽学園高校、自由ケ丘高校などがその対象です。
問題のレベルは、若干易しめに作成しているので、
・スーパー特進を志望する人は「全問正解」
・特進、準特進を志望する人は、「正答率80%」
・進学を志望するひとは、「正答率50%」
を目指して頑張ってください。
教科は、国語、数学、理科、社会、英語から大問1問ずつです。
まだ掲載していない教科は、随時UPします。
【問題】九産大付属九州産業高校入試対策問題
【数学】図のように。AB=6cm、BC=8cmの長方形ABCDがあり、∠Bの二等分線とCDの延長との交点をEとする。また、BEとAC,ADとの交点をそれぞれP,Qとする。このとき、次の問いに答えなさい。
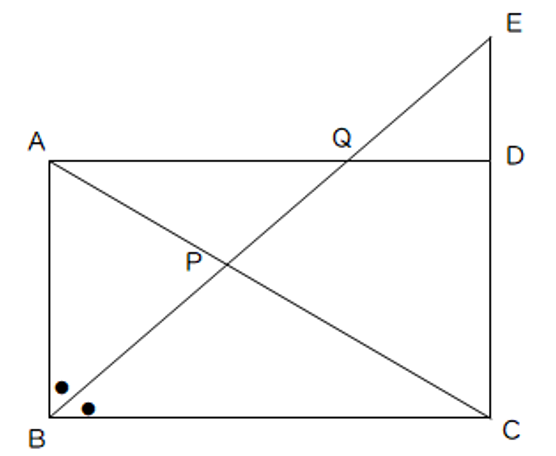
(1)EDの長さをそれぞれ求めよ。
(2)CPの長さをそれぞれ求めよ。
(3)四角形PQDCと三角形APBの面積比を求めよ。
【理科】A班からD班は、マグネシウムをステンレス皿に入れ十分に加熱する実験を行った。表はそのときの、加熱前のマグネシウムの質量と、生じた白い物質の質量を記録したものである。これについて、次の各問いに答えよ。
| A班 | B班 | C班 | D班 | |
| マグネシウムの質量〔g〕 | 0.3 | 0.6 | 0.9 | 1.2 |
| 白色の物質の質量〔g〕 | 0.5 | 1.0 | 1.5 | 2.0 |
(1)この実験から、マグネシウムと酸素は、質量比何対何で反応することが分かるか。最も簡単な整数比で答えよ。
(2)次にE班が、マグネシウム2.7gを同じように十分に反応させると、白い物質が生じた。この白い物質は何g生じたか。
(3)次にF班も同じように、マグネシウム1.5gを加熱したが、加熱の仕方が不十分だったため、加熱後の質量は2.1gにしかならなかった。未反応のマグネシウムは何gか。
(4)銅と酸素は質量比4:1で反応することが知られている。同じ質量の銅とマグネシウムと化合する酸素の質量比を答えよ。
【社会】下の表は基本的人権をまとめたものである。表を見て、問いに答えなさい。
| 平等権 | 法の下の平等など |
| 自由権 | ①身体の自由、(1 )、経済活動の自由 |
| (2 ) | 生存権、②教育を受ける権利、勤労の権利、労働三権 |
| 参政権 | 選挙権、被選挙権、直接請求権、国民審査、国民投票など |
| 新しい人権 | 環境権、プライバシーの権利、(3 )、自己決定権など |
(1)( )に適語を入れなさい。
(2)下線部①について、次のア~エでこれに当てはまるものを一つ選びなさい。
ア 自由にものを考えたり、信仰や思想を持つことができる。
イ 裁判所の令状なしに逮捕されることはない。
ウ 集会・結社や言論・出版などが自由にできる。
エ 自由に職業を選んだり、自分で得た財産を所有できる。
(3)下線部②が規定されているのは日本国憲法の第何条か、数字で答えよ。
【解説・解答】九産大付属九州産業高校入試対策問題
【数学】
<ポイント>
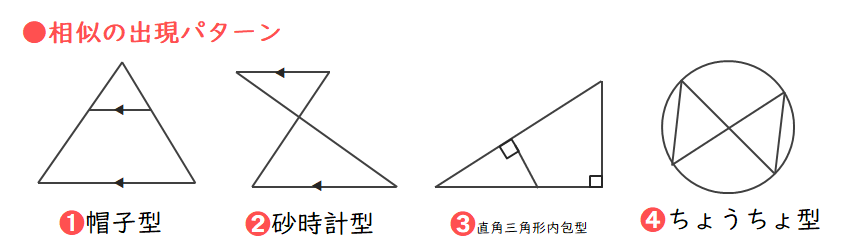
➊特に入試や実力テストでは「角を二等分する」、「二等分された角」などとあれば、角の二等分線定理を利用することが圧倒的に多い。
➋角の二等分線定理で単独で出題されることは少なく、合わせて相似や三平方の定理を途中組み合わせたり、使用させたりして解答させる。
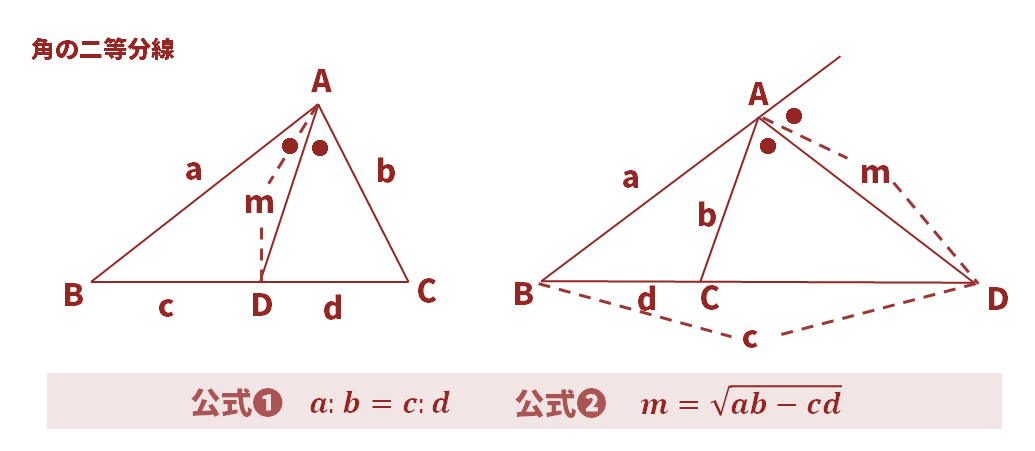
(1)EDの長さ
上の図の「相似の出現パターンの砂時計型」より、△AQB∽△DQEより、AB:DE=AQ:QDが成り立つので、DE=xとすると、6:x=6:2より、x=2cmとなる。
(2)CPの長さ
ACは、三平方の定理より、10cm。また、角の二等分線定理より、AP:AC=3:4よって、求めるCP=10×(4/7)となり、40/7cm
(3)四角形PQDCと三角形APBの面積比
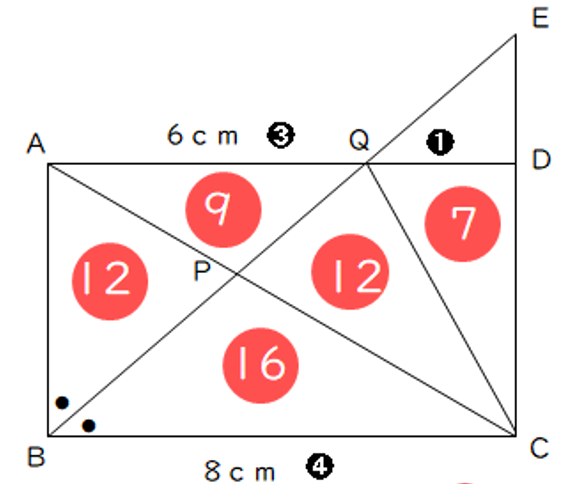
相似比の2乗は面積比を利用すると、四角形PQDC:三角形APB=19:12となる。
【解答】
(1)EDの長さ 2cm
(2)CPの長さ 40/7cm
(3)四角形PQDCと三角形APBの面積比 7:4
【理科】
(1)この実験から、マグネシウムと酸素は、質量比何対何で反応することが分かるか。最も簡単な整数比で答えよ。
3:2
どの班の結果を使っても同じになりますが、A班の結果で考えてみると、0.3gのマグネシウムが加熱後に0.5gになっています。
0.5-0.3=0.2
0.3gのマグネシウムに0.2gの酸素が化合しているので、
0.3:0.2=3:2
マグネシウム:酸素:酸化マグネシウム=3:2:5 は覚えておきましょう。
(2)次にE班が、マグネシウム2.7gを同じように十分に反応させると、白い物質が生じた。この白い物質は何g生じたか。
4.5g
マグネシウムと酸化マグネシウムの質量比は3:5なので、
3:5=2.7:x
x=4.5
(3)次にF班も同じように、マグネシウム1.5gを加熱したが、加熱の仕方が不十分だったため、加熱後の質量は2.1gにしかならなかった。未反応のマグネシウムは何gか。
0.6g
化合した酸素は、
2.1-1.5=0.6g
反応したマグネシウムは、
3:2=x:0.6
x=0.9g
未反応のマグネシウムは、
1.5-0.9=0.6g
(4)銅と酸素は質量比4:1で反応することが知られている。同じ質量の銅とマグネシウムと化合する酸素の質量比を答えよ。
銅と化合する酸素:マグネシウムと化合する酸素=3:8
銅:酸素=4:1
マグネシウム:酸素=3:2
ここで金属の比をそろえると、
銅:酸素=12:3
マグネシウム:酸素=12:8
したがって、同じ質量の銅とマグネシウムと化合する酸素の質量比は、
3:8
【社会】
(1)
1精神の自由
2社会権
3知る権利
(2)イ
(3)26条


コメント